炭酸水素ナトリウム
たんさんすいそなとりうむ
sodium hydrogencarbonate
炭酸水素ナトリウム(sodium hydrogen carbonate,sodium bicarbonate)$\ce{NaHCO3}$ は工業的にも生活にも,そして化学の学習にも非常に便利で使い勝手が良い化合物ですので,必ず身近などこかでお世話になっているはずです。毒性や環境負荷についてもほとんど気にする必要がない優れもので,性状は白色で無臭の固体です。炭酸の $\ce{H}$ が残っているので分類としては酸性塩(acid salt)ですが,水溶液は塩基性を示します。

炭酸水素ナトリウム(重曹)
身近なだけに別名がたくさんあって,やや古い言い方も含めると,重曹,重炭酸ナトリウム,重炭酸ソーダ,酸性炭酸ナトリウムというのはすべて $\ce{NaHCO3}$ のことです。炭酸水素ナトリウムよりは重曹の方がなじみがあるという方もいると思いますし,工業的には重曹という名称が一般的です。医療用医薬品(処方薬)としてはメイロン,プレビネートとも呼ばれています。
身の回りの重曹の用途をいくつか挙げると,胃薬のような一般用医薬品,洗剤,入浴剤,ベーキングパウダーなどに使われています。ベーキングパウダー(膨らし粉)は高校の化学でも扱われますが,ベーキングパウダーと重曹はイコールではありませんので注意してください。重曹は上の写真にもあるように英語で baking soda とも言うので,これが baking powder と混同しやすいのですが,両者は使い分けなくてはいけません。教科書でも「ベーキングパウダー(炭酸水素ナトリウムを含む)」のような記述になっています。ベーキングパウダーとしてではなく,重曹そのものも調理に用いられます。韓国ドラマの「イカゲーム」で話題になったカルメ焼きを作るのにも使われます。
身近というと語弊があるかもしれませんが,消火剤としても使われています。消火器から白い粉が噴き出すのを消火訓練などで見たことがある方もいると思います。これが重曹ですと言いたいところですが,現在出回っている粉末消火器はほとんどが ABC 火災(A : 普通,B : 油,C : 電気)対応型で,これには薄いピンク色に着色されたリン酸塩が入っていますので,訓練後にピンク色が残っていたら,残念ながらそれは重曹ではありません。ABC 火災型とは別に BC 火災に特化した消火器があって,こちらに重曹が使われています。使用後に白色または薄い緑色が残っていれば重曹の可能性大です。油脂火災などで出動する化学消防車の粉末消火剤にも用いられますので,こちらの映像を見る機会の方が多いかもしれません。工業的には洗浄剤や他の化学製品の原料として用いられるほか,酸や酸性ガスの中和剤としての用途もあります。
工業的な製造方法
炭酸水素ナトリウムはナーコ石(nahcolite)という単斜晶系の透明感のある白色の結晶からなる鉱物として天然に産出します。$\ce{NaHCO3}$ だから NaHCO = nahco(ナーコ)という素直なネーミングです。

ナーコ石
(Rob Lavinsky, iRocks.com – CC-BY-SA-3.0, CC BY-SA 3.0, via Wikimedia Commons)
ナーコ石を原料とした重曹は天然重曹の呼び名で市販されています。鉱物を掘り出してきたものなので,添加物フリーと書いてあっても,もともと不純物が含まれている可能性はあります(精製はしていると思いますが)。
一方,炭酸ナトリウム(ソーダ灰)$\ce{Na2CO3}$ や水酸化ナトリウム(苛性ソーダ)$\ce{NaOH}$ の水溶液に二酸化炭素を吸収させて重曹を製造することもできます。炭酸ナトリウムを用いた場合は熱分解の逆反応が起こり,炭酸ナトリウムよりも溶解度が小さい重曹が沈澱します。水酸化ナトリウムも溶解度が大きいので,二酸化炭素の吸収により重曹が沈澱します。水酸化ナトリウムは電解法により高純度のものが得られますので,国内の製造プロセスではこちらの方式により重曹の高純度化が実現されています。
これらの方法で製造された重曹は工業製品なので天然を謳うことはできませんが,国内の工場で製造されたものであれば国産重曹ですし高純度です。天然の不純物が含まれているかもしれない天然重曹と,純度の高い工業製品の国産重曹。もちろん食品添加物用のものであればどちらも調理に使って問題ありませんのでお好みでどうぞ。不純物という言葉に警戒心を持たれた方は「天然のミネラル」ととらえていただければ安心していただけるでしょうか。
一般工業用の重曹というのもあって,こちらはヒ素や重金属といった不純物の混入が基準値以下であることを保証しないので調理に使ってはいけません。ただし,検査しないだけで,これらの有害物質が入っているという意味ではありません。国内製造のものであれば製造プロセスは他のグレードと共通で,実質同じものだと試薬会社から聞いたことがあります。検査代がかからないので安くなります。掃除用として市販されているものがどちらを原料としているかは分かりませんが,恐らく価格が安い工業用を使っていると思いますし,製造プロセスが異なる外国産の可能性もありますので,調理用に流用するのはやめておいた方が安心です。
なお,炭酸ナトリウムの製造プロセスであるアンモニアソーダ法(ソルベー法)の中間生成物として $\ce{NaHCO3}$ を取り出すこともできますが,現在この方法を採用している国内メーカーはありません。また,トロナ(trona)として天然に産出する鉱物 $\ce{NaCO3.NaHCO3.2H2O}$(物質名としてはセスキ炭酸ナトリウム二水和物といい炭酸ナトリウムと炭酸水素ナトリウムからなる複塩です)を原料とすることもできます。輸入物の重曹はこちらの製造プロセスの可能性があります。
炭酸水素ナトリウムの反応
固体状態では加熱により $50\oC$ くらいから熱分解が始まり,$270\oC$ 以上では無水炭酸ナトリウムになります。
また,塩酸などの酸と反応すると二酸化炭素が発生します。この反応は強酸によって弱酸である炭酸が遊離し,それがさらに水と二酸化炭素に分解したものと考えられます。
水酸化ナトリウムとの反応では炭酸ナトリウムが生成します。
この反応は炭酸水素イオン $\ce{HCO3-}$ と水酸化物イオン $\ce{OH-}$ との中和反応です。
炭酸水素ナトリウムの溶解度
炭酸水素ナトリウムは水にまったく溶けないということはありませんが,溶解度は比較的小さめで,$25\oC$ の水 $100\unit{g}$ に $10.3\unit{g}$ 程度溶けます。食塩が同温同量の水に約 $36\unit{g}$ 溶けますので,感覚としては,まあまあ,ほどほどに溶けるという感じです。なおメタノールには難溶,エタノールとジエチルエーテルには不溶です。
下の図は赤線が炭酸水素ナトリウムの溶解度曲線(水 $100\unit{g}$ に対して溶ける最大の炭酸水素ナトリウムの質量($\mathrm{g}$)),緑線が飽和水溶液の質量パーセント濃度の温度依存性を示したものです。縦軸の目盛りは共通です。温度が高い方が溶解度は大きくなりますが,水溶液では $65\oC$ を超えたくらいから徐々に炭酸ナトリウムと二酸化炭素に分解します。
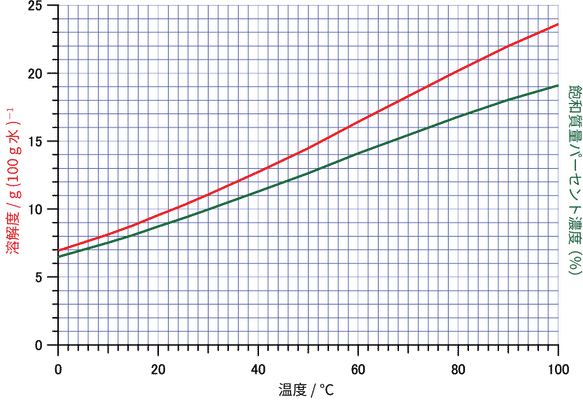
$\ce{NaHCO3}$ の水への溶解。赤:水 $100\unit{g}$ に対して溶解する質量(溶解度),
緑:飽和溶液の質量パーセント濃度(飽和溶液 $100\unit{g}$ に含まれる溶質の質量($\mathrm{g}$))
重曹水溶液の $\pH$
炭酸水素ナトリウムの水溶液の $\pH$ を求める方法については講義編(酸・塩基)の pH 計算の実際(両性電解質)で解説していますのでそちらをご覧ください。ここでは結論だけを書くと,重曹水溶液は一定以上の濃度であれば,濃度に関係なく $\pH$ は一定値 $8.35$ 程度になります。この $\pH$ はフェノールフタレインの変色域にぎりぎりかかるかかからないかの境目で,薄くしか呈色しませんので,重曹水溶液は塩基性ですが,フェノールフタレインで検出するのはなかなか難しいです。炭酸ナトリウムであればフェノールフタレインは赤色に変色します。
重曹水溶液の $\pH$ が飽和溶液でもほどほどの塩基性に収まるというのは便利な性質で,実験室で酸を処分する際に中和して廃棄しますが,水酸化ナトリウムのような強塩基を用いると,入れすぎたときに再び酸を追加して $\pH$ を調整しなくてはならず,面倒で無駄が生じます(ただし二酸化炭素が生じないとか,単位重量当たりに中和できる量が多くなるなどの利点もある)。重曹であれば入れすぎても $\pH$ が基準内に収まりますので安心です。
芳香族化合物の安息香酸(benzoic acid)とフェノール(phenol)が溶解したエーテル溶液を重曹水溶液で分液すると,安息香酸のみがナトリウム塩として水相に抽出されると高校の化学で学習しますが,ここでも重曹水溶液の $\pH$ が濃度によらずほぼ一定に保たれる性質が利用されています。
参考
- カルメ焼きレシピ(クックパッド)
- AGC 株式会社ウェブサイトより
最終更新日 2025/06/26

