錯体の異性体
錯体には幾何構造,配位子の配位様式などの違いにより,各種の異性体が存在します。
- 連結異性(linkage isomerism),結合異性
$\ce{[Co(NH3)5(NO2)]^{2+}}$の $\ce{NO2}$ は,酸素原子がコバルトイオンに配位する赤色の $\kappa O$ 体($\ce{Co-O}$)と,窒素原子が配位する黄色の $\kappa N$ 体($\ce{Co-N}$)の 2 種類が存在し,これを連結異性または結合異性といいます。連結異性を区別する用語として,thiocyanato と isothiocyanato,および nitroと nitrito の用法は旧ルールで,新ルールでは thiocyanato-$\kappa S$($\ce{SCN-\kappa\textit{S}}$)と thiocyanato-$\kappa N$($\ce{SCN-\kappa\textit{N}}$) および nitrito-$\kappa N$($\ce{NO2-$\kappa$\textit{N}}$)と nitrito-$\kappa O$($\ce{NO2-\kappa\textit{O}}$)で区別します。ただし,旧ルールも依然として使用されています。 - イオン化異性(ionization isomerism)
$\ce{[PtCl2(NH3)4]Br2}$ と $\ce{[PtBr2(NH3)4]Cl2}$ は溶液中で異なるイオンになります。 - 水和異性(hydration isomerism)
$\ce{CrCl3.6H2O}$ には $\ce{[Cr(OH2)6]Cl3}$,$\ce{[CrCl(OH2)5]Cl2.H2O}$,$\ce{[CrCl2(OH2)4]Cl.2H2O}$ の 3 種の水和異性体が知られています。 - 配位異性(coordination isomerism)
$\ce{[Co(NH3)6][Cr(CN)6]}$ と $\ce{[Cr(NH3)6][Co(CN)6]}$ は,アンミン配位子とシアニド配位子が配位する金属イオンがそっくり入れ替わっています。このような関係にある構造を配位異性といいます。
幾何異性
複数種類の配位子が一つの金属イオンに配位するとき,幾何学的構造が異なる異性体が生じることがあり,これを幾何異性体(geometrical isomer)といいます。
- cis-,trans - 異性
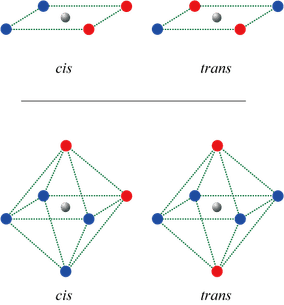
$\ce{[Pt^{II}Cl2(NH3)2]}$ などの平面四配位 $\ce{[MA2B2]}$ 型の構造では,$\ce{A}$ どうし,$\ce{B}$ どうしが隣り合った cis 体と,向かい合った trans 体の2種の異性体が存在します。一方,四面体配位の場合は cis,trans 異性は存在しません。$\ce{[Co^{III}Cl2(NH3)4]+}$などの六配位正八面体 $\ce{[MA4B2]}$ 型では,$\ce{B}$ が隣り合うものが cis 体,金属 $\ce{M}$ を介して反対側にあるものが trans 体です。
- fac-,mer - 異性
六配位正八面体 $\ce{[MA3B3]}$ 型で,三つの $\ce{A}$,$\ce{B}$ が金属 $\ce{M}$ を含まない平面内にあるものを fac 体(facial),金属 $\ce{M}$ を含む平面内にあるものを mer 体(meridional)といいます。

- 鏡像異性(optical isomerism)
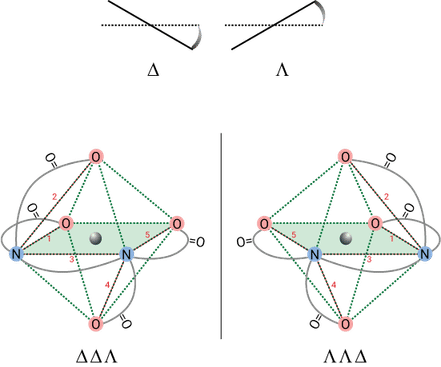
六配位正八面体構造において,2 座配位子で,3 回軸方向から見たときに連結した配位子が時計回りになるものを $\Delta$ 体,反時計回りになるものを $\Lambda$ 体といいます。
より厳密には,ねじれの関係にある 2 本の稜線が反時計回りの関係にあるものを $\Delta$,時計回りの関係にあるものを $\Lambda$ と定義します。この方法に基づくと,下図の左に示した EDTA 錯体は稜線 1 と 4,2と 5,2と 4 がねじれの関係にあり,それぞれ $\Delta$,$\Delta$,$\Lambda$ となるので,$\Delta\Delta\Lambda$ 体と書きます。